来源:医药观澜
中国国家药监局(NMPA)药品注册进度查询结果最新公示,基石药业申报的RET抑制剂普拉替尼(pralsetinib)新药上市申请(NDA)审评审批状态已更新为:在审批。公开资料显示,该药本次申请的适应症为既往接受过含铂化疗的RET基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。值得一提的是,如果该药获批,它将有望成为中国首个获批的RET抑制剂。
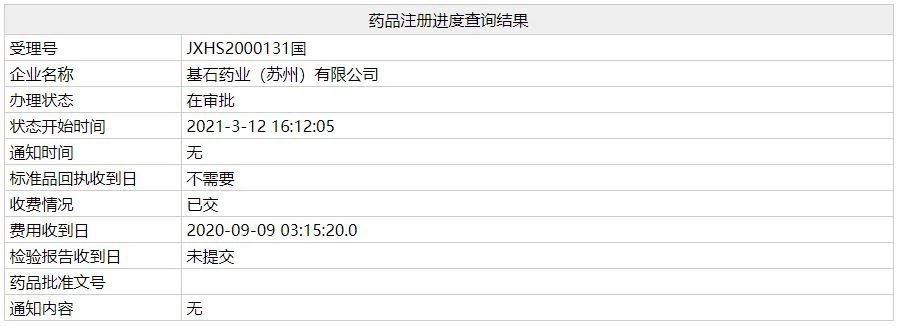
截图来源:NMPA官网
普拉替尼是Blueprint Medicines开发的一款强效、高选择性靶向致癌性RET变异(包括可预见的耐药突变)的口服精准疗法,基石药业于2018年6月获得了该产品在大中华区的独家开发和商业化授权。在美国,该药已被FDA批准用于治疗转移性RET融合阳性NSCLC的成人患者、需要系统性治疗的晚期或转移性RET突变甲状腺髓样癌成人和12岁及以上儿童患者,以及需要系统性治疗且放射性碘难治(如适用)的晚期或转移性RET融合阳性甲状腺癌成人和12岁及以上儿童患者。
在中国,普拉替尼的上市申请于2020年8月被中国国家药监局药品审评中心(CDE)纳入优先审评,拟用于既往接受过含铂化疗的转染重排(RET)融合阳性的局部晚期或转移性NSCLC患者的治疗。
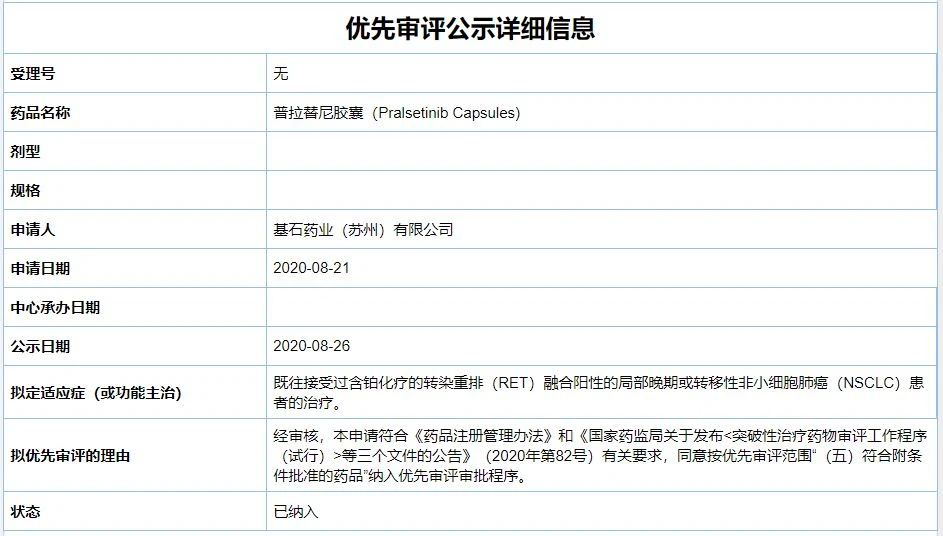
图片来源:CDE官网
根据公开资料,普拉替尼的这项上市申请是基于一项开放标签、多中心的全球性1/2期临床试验,该研究旨在评估普拉替尼在RET融合阳性NSCLC的晚期实体瘤患者中的安全性、耐受性和有效性。研究数据显示,普拉替尼在经含铂化疗的RET融合阳性的NSCLC中国患者中显示出了优越和持久的抗肿瘤活性,总体缓解率(ORR)为56%,安全性及耐受性良好,未出现与普拉替尼相关的不良事件导致的终止治疗或死亡。
注:原文有删减
*声明:本文由入驻新浪医药新闻作者撰写,观点仅代表作者本人,不代表新浪医药新闻立场。▽关注【药明康德】微信公众号

- 没有相关新闻!
①医疗在线上发布的所在信息未经本网授权,不得转载、摘编或利用其它方式使用。已经本网授权使用作品的,应在授权范围内使用,并注明“来源:医疗在线”或“来源:http://www.120eyes.com”。违反上述声明者,本网将追究其相关法律责任。
②本网转载其他媒体稿件是为了传播更多的信息,此类稿件不代表本网观点。如果本网转载的稿件涉及您的版权、名誉权等问题,请尽快与本网联系,本网将依照国家相关法律法规尽快妥善处理。








